
「医线」是创业邦推出的医疗健康系列栏目,立足医疗健康一线,捕捉行业内最新动态,洞察创投新趋势。
医线周报,为你挑选过去一周(10.23~10.29)最值得关注的「医线」新闻。
整理丨高嵩
Part.1、一周投融资
本周全球医疗健康领域融资事件共16起,其中国内11起,国外5起。据睿兽分析不完全统计,本周国内医疗融资金额总计超过33亿人民币,海外融资金额总计达2.44亿美元。

数据来源:睿兽分析
本周国内融资超1亿人民币的公司信息如下:
维立志博生物是一家临床阶段的生物制药公司,由资深留美抗体药物研发团队在南京创立。致力于具有自主知识产权的治疗肿瘤和其他重大疾病的抗体新药研发,聚焦尚未满足的医药需求,特别是肿瘤免疫治疗面临的问题和挑战。公司在单靶点抗体和双特异性抗体新药研发技术平台上,已经拥有十多个新型肿瘤免疫治疗抗体项目组成的丰富研发管线。
亘喜生物亘喜生物成立于2017 年,旨在攻克行业所面临的自体和同种异体CAR-T细胞产品普遍存在的技术挑战。公司科学家自主研发出前沿的FasTCAR和TruUCAR技术平台。基于FasTCAR平台技术,亘喜生物开发出表型更年轻、耗竭更少、杀伤更佳的自体CAR-T细胞产品。该T细胞经22~36 小时生产,能够在次日收获;基于TruUCAR平台技术,亘喜生物开发出源自无需HLA配型的健康供体的T细胞的通用型CAR-T产品。
普实医疗是一家医疗器械产品研发生产商,主要从事开发医疗设备技术以及生产及销售医疗设备,专攻心脏相关疾病,其产品以PushMed商标营销及销售。
质肽生物是一家医学研究与试验发展服务提供商,主要经营范围是技术开发、技术服务;医学研究与试验发展;经济信息咨询等。
臻和科技全称无锡臻和生物科技有限公司,成立于2014年,是一家以二代测序技术和生物信息学为核心,从事无创为主的肿瘤个体化精准诊疗和伴随诊断的企业,其产品包括百适博、耀适博、派蒂万、玛普润、MammaPrint等。
联新成立于2010年,定位于为医院提供智慧病房和慢病管理解决方案,并且从临床实际需求出发,为医院量身打造了一系列智能化产品,帮助医院建立覆盖诊断治疗、临床护理、患者服务、药品物品管理、质量管理等5个不同维度的全院全业务信息化管理体系,实现医院应用业务从传统手段向智能化手段的过渡,提升医院整体运营管理水平。
苏州圣诺是直属美国圣诺制药集团(Sirnaomics,Inc.)的一家临床阶段生物制药公司,利用其在RNA干扰(RNAi)技术方面的卓越知识和经验,根据临床医疗市场需求,针对临床上目前没有或无有效药物的疾病指证进行药物发现和开发,开辟高价值的新药创制之路。自创建以来聚焦核酸干扰药物导入平台建设和新药品种研发创制,目前已成为全球唯一具备在中美同时推动核酸干扰新药进入临床研究能力的企业,推动我国核酸干扰创新药临床试验“零”的突破。
国外融资情况如下:
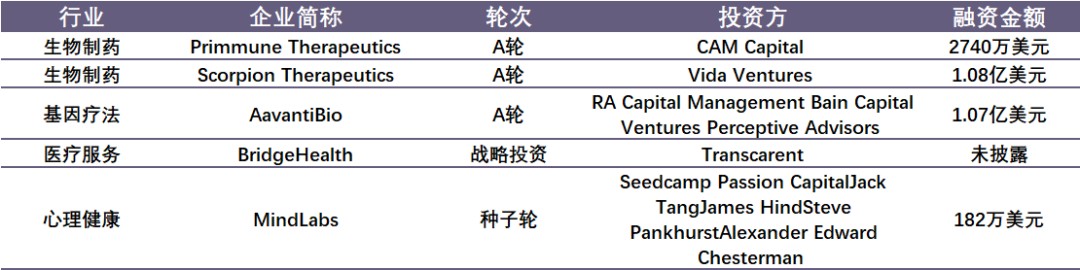
数据来源:睿兽分析
Part.2、一周政策动向
关键词: 医院重点监控、超过500家医院部署5G医疗、5年中央公共卫生投资达1415亿元;慢性病复诊费用纳入医保报销
国家药监局点名,100家医院遭重点监控,全国撒网
10月27日,国家药监局发布通知,宣布对100家医疗机构的药物滥用情况进行监测,其中包括大批综合大三甲医院。这些医院是经过专家评审选出,作为国家药物滥用监测哨点,进一步完善了中国药物滥用监测体系。
这里的药品滥用是指反复、大量地使用具有依赖性特性或依赖性潜力的药物,属于非医疗目的用药。
从国家药监局近年来的报告情况看,除了海洛因、合成毒品之外,医疗用药品,包括医用麻醉药品、医用精神药品,甚至复方地芬诺酯、复方甘草片、止咳水、感冒药等非管制的常用药,也存在被滥用的风险。(健识局)
国家卫健委:中央5年投资1415亿元支持公卫事业
10月28日,国家卫生健康委员会副主任于学军在国新办发布会上介绍,2016年—2020年国家累计安排中央预算内的投资1415亿元支持包括像疾控中心建设等8000多个公共卫生的医疗项目,这比“十二五”总投资增加了23%。
国家卫健委:超过500家医院已经部署5G网络
10月28日,从国家卫健委获悉,我国正在二级以上医院推进智慧医院建设,目前已有超过500家医院部署5G网络,并且开展了5G医疗应用试点。
智慧医院建设主要包括针对医务人员的“智慧医疗”、针对患者的“智慧服务”以及针对医院的“智慧管理”。国家卫健委要求,各地医院推进以电子病历为核心的医院信息化建设,提升临床诊疗工作的智慧化程度。以“智慧服务”建设为抓手,为患者提供覆盖诊前、诊中、诊后的全流程、个性化、智能化服务,改善患者就医体验。
截至目前,全国已有7800家医院实现线上结算;3680家医院能够提供就诊提醒、检查检验报告信息推送等服务。三级医院网上预约诊疗率已达50%以上,3300家医院将分时段预约诊疗精准到30分钟。(央视新闻)
14部门发文:将慢性病互联网复诊费用纳入医保支付范围
近日,国家发改委等14部门印发《近期扩内需促消费的工作方案》(下称《方案》)。《方案》提到,推动线下服务消费加速“触网”,充分释放线上经济潜力。要完善“互联网+”医保支付政策。在保证医疗安全和质量前提下,将慢性病互联网复诊费用纳入医保支付范围。
Part.3、大公司&大事件
华北制药董事长辞职
10月26日,华北制药发布公告称,公司董事会于2020年10月26日收到公司董事长杨国占的书面辞职报告。

杨国占因工作原因,向董事会申请辞去公司董事、董事长职务,同时一并辞去公司董事会战略(投资决策)委员会主任委员和提名与薪酬考核委员会委员职务。辞去上述职务后,杨国占将不再担任华北制药任何职务。
根据公告,杨国占的辞职报告已经生效,在华北制药选举出新任董事长之前由副董事长刘文富主持董事会工作。(公司公告)
13亿美元交易达成!基石药业授权EQRx开发舒格利单抗和CS1003
10月27日,基石药业宣布与EQRx达成全球战略合作,将独家授权EQRx在大中华区以外地区开发和商业化舒格利单抗(CS1001,抗PD-L1单抗)及CS1003(抗PD-1单抗)这两款处于后期研发阶段的肿瘤免疫治疗药物。EQRx拥有创新的商业模式,将助力这两款药物在目标适应症上相对于现有疗法具备全球市场的竞争优势。
根据协议条款,基石药业将获得1.5亿美元的首付款,及最高可达11.5亿美元的里程碑付款以及额外的分级特许权使用费。EQRx将获得舒格利单抗和CS1003在除中国大陆、台湾、香港和澳门地区以外全球市场的独家商业化权利。基石药业将保留CS1003在大中华区的开发和商业化权利,并将继续探索其作为单药和联合疗法的骨架产品的发展前景。(医药魔方)
陈启宇辞任复星医药董事长,复星医药管理层大调整
10月29日,复星医药发布公告称,因工作安排调整,陈启宇、姚方分别辞去董事长、联席董事长职务,该人事变动当天生效。同时,复星医药宣布吴以芳接任董事长职位,并担任执行董事和首席执行官。吴以芳此前为复星医药总裁兼首席执行官。
此外,复星医药当天还宣布了一系列任命:聘任陈玉卿、王可心、李东明为联席总裁,关晓晖为执行总裁兼首席财务官;聘任文德镛、王冬华为高级副总裁。(公司公告)
天士力总经理辞职
10月29日,天士力发布公告称,董事会于近日收到朱永宏的书面辞职报告——因公司战略发展与组织团队建设,朱永宏申请辞去公司总经理职务,辞职后仍继续担任公司董事职务。

同时,通过天士力董事会提名,薪酬与考核委员会审议,聘任苏晶担任新的总经理。
公开资料显示,苏晶曾经是北京协和医院基本外科医生,也曾做过默沙东(中国)有限公司北区销售推广经理,于2003年加入天士力,其在天士力曾先后担任营销集团市场策划板块总经理、轮值总经理,天士力副总经理、常务副总经理。目前,苏晶是天士力的现任董事、总经理,同时还兼任天津天士力医药商业有限公司董事、总经理等职务。
不同于多年投身市场营销一线的新任总经理,天士力前任总经理朱永宏来自于研发和生产领域。
资料显示,朱永宏是中药学博士,注册执业药师,还享受国务院特殊津贴,其曾任天津天士力集团有限公司董事长助理兼研究院副院长、天士力控股集团有限公司副总裁兼生产制造事业群首席执行官、天士力副董事长。(赛柏蓝)
Part.4、新产品&新技术
恒瑞 PD-1 联合阿帕替尼 III 期临床获批,用于肝细胞癌术后辅助治疗
10 月 23 日,恒瑞医药发布公告称,公司近日收到 NMPA 《药物临床试验批准通知 书》,批准其 PD-1 单抗卡瑞利珠单抗联合阿帕替尼用于肝细胞癌(HCC)根治性手术或消融后伴高复发风险人群的辅助治疗。恒瑞将于近期开展此项 III 期临床试验。(医药魔方)

药监局受理首个基因编辑临床试验
10月27日,基因编辑科技企业博雅辑因宣布,国家药品监督管理局药品审评中心(CDE)已受理其针对输血依赖型β地中海贫血的基因编辑疗法产品ET-01的临床试验申请。
这是中国首个获得受理的基因编辑疗法临床试验申请,根据国家药监局规定,还须经过60个工作日默示许可,方为正式获批临床试验。目前具体临床试验方案,包括纳入患者数量、治疗时间、试验地点等尚未披露。
该临床试验计划在输血依赖型β地中海贫血患者中评价ET-01单次移植的安全性和有效性。具体来讲,ET-01疗法采用CRISPR/Cas9基因编辑技术,通过采集患者自体动员外周血单个核细胞,在富集CD34+细胞群后通过前述技术编辑BCL11A基因的红系增强子制成注射液。(企业信息)
正大天晴/康方生物 PD-1 三线治疗转移性鼻咽癌获 FDA 快速审批通道资格
10 月 27 日,中国生物制药发布公告,其与康方生物合作的抗 PD-1 单抗「派安普利」(商品名:安尼可;研发代号:AK105)用于三线治疗转移性鼻咽癌,获得美国 FDA 授予快速审批通道资格(FTD),将显著的支持并加速派安普利单抗在美国的商业拓展计划。

FDA 的快速审批通道旨在加速或促进用于治疗当前并无有效治疗方案的严重或危及生命的疾病或病情、且展示出有满足这一疾病当前未被满足的医疗需求潜力的新药的评审过程。具 FTD 的候选药物有资格与 FDA 进行更频繁的沟通、参与优先评审(如果符合相关标准)及参与新药申请的滚动评审。这将加快相关药物的开发及上市进程。(Insight数据库)
罗氏 T+A 免疫联合治疗在国内获批,用于肝细胞癌
10 月 28 日,罗氏宣布 NMPA 批准其肿瘤免疫创新药物阿替利珠单抗(商品名:泰圣奇®,Tecentriq®)联合贝伐珠单抗(「T+A」联合疗法)用于治疗既往未接受过系统治疗的不可切除肝细胞癌(HCC)患者。此次获批的主要依据是 III 期临床试验 IMbrave150 的研究结果,其中包括对 194 名中国亚群患者的分析。(Insight数据库)
Part.5、言论&数据
半壁江山!中国新药许可交易数量激增,创新药企“十字路口”何去何从?
中国生物制药行业在2019年创下了全球生命科学领域的投资交易纪录之后,在2020年又相对平安无事地度过了新冠肺炎疫情的侵袭。在风投热钱的推动下,人们对创新疗法的兴趣越来越大,特许经营、授权合作和合资企业等相关交易量也随之大幅增加。来自GBI的数据显示,今年1-8月全球生物医药行业共签署了287笔交易,总规模为123.5亿美元,有望创下年度新高。
值得关注的是,随着中国本土生物技术公司研发能力不断增强,参与全球交易也越来越活跃。在今年前8个月,来自中国公司的交易贡献了近一半的价值规模。其中,在新冠肺炎疫苗研发领域,出现了27笔中国公司和海外公司的合作研发交易。
GBI数据显示,截至2020年8月31日,许可、合作和合资企业三类交易总规模为123.5亿美元,2019年全年交易规模为138亿美元,今年有望创下年度新高。
截至2020年8月31日,全球生物医药行业共发生了287笔交易,其中189笔集中在制药领域,较2019年同期公布的241笔交易增长19%,而2019年并没有受到新冠肺炎的影响。本次GBI统计的交易数据,既包括产品权利的直接许可/收购,也包括以终止产品许可证为目的的研发合作(例如用于评估组合疗法)。
在今年前8个月,中国生物技术公司外包许可交易激增,反映出越来越多具有创新能力和高质量产品的中国本土生物技术公司为全球市场做出贡献。在今年前8个月发生的189个生物制药交易中,有102个是引入许可证和合作交易,有44个是来自中国的许可交易。从交易规模上看,这44笔交易的总价值为53.8亿美元,而102个引入许可和合作交易的总价值为62.6亿美元,远远领先于2019年15亿美元的对外交易规模。
今年前1-8月,特许经营许可证协议交易总规模为62.6亿美元,略低于2019年同期的87亿美元。
本文为创业邦原创,未经授权不得转载,否则创业邦将保留向其追究法律责任的权利。如需转载或有任何疑问,请联系editor@cyzone.cn。












